Les clés pour réussir ses audits internes !
Publié le mardi 10 janvier 2023

Trop souvent bâclés, les audits internes peuvent constituer un véritable levier pour initier l’amélioration continue en entreprise, mais pourquoi n’est-ce pas toujours le cas ?
Au lieu d’être considéré comme un outil constructif permettant de développer l’implication et l’esprit critique des collaborateurs, ils sont souvent perçus comme une obligation normative. Dans ce cas, des éléments essentiels au bon déroulement des audits internes sont alors négligés et cela peut engendrer des craintes de la part des collaborateurs, tel que le sentiment d’être jugés personnellement.
Bien plus qu’un simple temps de questions-réponses, l’audit interne intègre également une partie de préparation et une partie de restitution/analyse des constats d’audit. Chacune de ces étapes doit faire l’objet d’une planification.
Pour tendre vers des audits internes constructifs, il est indispensable de valoriser les 4 éléments suivants :
- Sensibiliser les audités ainsi que la ligne hiérarchique sur le fait que les audits ne visent pas à juger les collaborateurs mais à évaluer la pérennité de nos activités pour consolider nos systèmes de management.
- Encourager la transparence des auditeurs avec les audités en partageant les éléments qui leurs semblent critiques, au fur et à mesure de l’entretien d’audit. Cela permettra d’éviter « l’effet surprise » lors de la séance de clôture.
- L’audit est un exercice de collaboration entre audités et auditeurs : l’audité apporte une expertise métier, tandis que l’auditeur apporte une expertise sur des techniques d’audit pour challenger l’existant.
- Les auditeurs doivent être sensibles à la dimension humaine afin de savoir réagir face aux différents comportements d’audités parfois stressés.
Pour conclure, mon expérience personnelle m’a démontré que nous faisons encore trop souvent l’erreur d’associer le bon déroulement d’un audit au nombre de non-conformités détectées. Cependant, si l’audit a pour but de fournir une évaluation la plus proche possible de la réalité, ne serait-il pas plus juste que le bon déroulement de l’audit repose sur la transparence et la collaboration des auditeurs et des audités ?
Article rédigé par Margot Medjo’o, Responsable pédagogique en SMI
Le développement durable est incontournable
Publié le jeudi 17 novembre 2022

En cette fin d’année, la situation internationale est complexe. Après deux années de pandémie, qui a mis sous tension la supply chain internationale, le monde se réveille avec crise énergétique, de l’instabilité économique auxquelles s’ajoute le grand défi de ce XXIème siècle, le changement climatique.
Dans ce contexte, le développement durable n’est plus un choix ou un effet de mode, mais un axe incontournable que devrait intégrer chaque organisation dans sa stratégie. Le FOREP – Forum Excellence & Performance – qui a eu lieu le 3 novembre dernier à Lausanne, a donné une vue d’ensemble de cette thématique. Les solutions aux défis qui nous font face sont multiples et relèvent de la société civile, des gouvernements et des entreprises. Madame Adèle Thorens, Conseillère aux États pour le Canton de Vaud, a abordé le sujet sous l’angle réglementaire. Après le refus du peuple de la loi CO2 en 2021, de nouvelles mesures sont en cours d’élaboration comprenant notamment la facilitation de l’économie circulaire. Monsieur Zouhair Aïch d’ARIAQ a donné un exemple concret d’application d’économie circulaire dans le secteur des semiconducteurs. L’association Ecoparc met en avant les standards ISO14001 et ISO45001, comme la norme ISO26000 qui détermine comment les organisations peuvent contribuer au développement durable. Pour ce faire, les entreprises doivent intégrer dans leurs vision et stratégie le développement durable comprenant notamment la gestion environnementale ou encore énergétique.
Des solutions il y en a, et elles sont multiples et variées. En définitive, le développement durable, à l’instar de la qualité, part d’une prise de conscience et se poursuit avec une stratégie, un plan d’actions et s’ancre dans l’organisation avec le changement d’un état d’esprit.
Les nouvelles formations sur les Dispositifs Médicaux (DM) dispensées chez ARIAQ
Publié le lundi 5 septembre 2022

Ce que vous devez savoir sur les formations ARIAQ des Dispositifs Médicaux
Il existe des changements importants dans la législation européenne applicable aux Dispositifs Médicaux. La réglementation de l’UE sur les dispositifs médicaux (Medical Devices Regulation, MDR) a remplacé les Directives MDD 93/42/CEE et AIMDD 90/385/CE et impose de nouvelles exigences aux fabricants et autres opérateurs économiques.

Répondant à la demande et aux besoins spécifiques des fabricants de dispositifs médicaux, l’institut ARIAQ propose deux cursus de formation certifiant à 3 niveaux et en parallèle ciblant les très nombreuses exigences particulières d’un domaine où les mutations sont rapides et nombreuses. La formation ARIAQ, unique sur le marché, se veut avant tout pratique. Elle est donc animée par des praticiens, experts dans leur domaine, qui amèneront les participants à acquérir l’essentiel des compétences requises par les professionnels du secteur.
Les principaux avantages des formations ARIAQ certifiantes sur les DM
Les formations Certifiantes ARIAQ sur les dispositifs médicaux sont conçues pour introduire les fabricants de dispositifs médicaux et autres opérateurs économiques dans la chaîne d’approvisionnement, aux changements clés des exigences pour le marquage CE suite à la publication du nouveau Règlement.
Les ordres de fabrication et leur ordonnancement
Publié le lundi 15 août 2022

L’ ordre de fabrication
Un OF, pour Ordre de Fabrication ou Order Manufacturing en anglais, est un terme utilisé pour autoriser l’ordonnancement de la production d’un produit ou d’une pièce, dans un atelier de fabrication.
Véritable lien opérationnel entre la commande client et la production, un ordre de fabrication est le déclencheur d’un nombre important d’activités au sein d’une entreprise. Pour tout responsable de fabrication, gérer la production peut s’avérer complexe en fonction des matières premières utilisées, des produits déjà planifiés, d’une quantité à fabriquer ou de la sous-traitance.
Chaque OF est associé à une gamme et une nomenclature produit. Il indique la quantité spécifique à produire, la date de lancement, la date demandée.
L’importance de l’exactitude des données techniques
L’exactitude des données techniques telles que les nomenclatures, les gammes opératoires, les postes de travail ou encore les temps de passage d’une opération de sous-traitance sont primordiaux pour une bonne vision future. Une erreur d’un temps unitaire dans une gamme opératoire peut en effet fausser toute la vision future de la charge / capacité une fois multipliée par la quantité de l’OF.
Les objectifs d’un OF
-
Respecter les commandes clients en temps et en heure : Grâce une cadence de production maîtrisée, l’OF permet d’éviter les retards de livraison et les rebuts d’un produit fini.
-
Maîtriser sa planification : à l’aide de son système ERP, le responsable de production pourra planifier et tracer efficacement, avec comme base de départ les OF.

L’ordonnancement et la priorisation des OF
-
L’ordonnancement ou Scheduling en anglais – désigne le procédé par lequel des priorités successives sont données à des tâches différentes. Les principaux composants de l’ordonnancement sont la direction de planification, la capacité des ressources et l’optimisation des matières.
-
Selon le type de priorités fixées (réduction des en-cours, réduction des tailles de lots, amélioration du taux de service), une règle de priorité est utilisée, les principales règles :
– FIFO (premier entrée, premier sortie)
– LIFO (dernier entrée, premier sortie)
– TFL (Temps de Fabrication le plus long)
– TMC : temps de la marge croissante par OF
– RC : ratio critique, on calcule le ratio de la marge par OF
Ariaq vous accompagne dans le développement de vos compétences ou celles de vos collaborateurs en ordonnancement de production.
Contactez-nous pour en discuter. Au plaisir d’en parler avec Vous !

Formation et conseil en Supply Chain
Mécanicien de Machines et Technicien ES en Exploitation & Logistique, Tonino a acquis au cours de son parcours professionnel une grande expérience en gestion de projets industriels, en planification de production et ordonnancement, achats stratégiques et composants mécaniques, et gestion de stock. Passionné par l’amélioration continue il aime rechercher les failles afin de trouver des solutions optimales en tenant compte du terrain et des besoins techniques.
Identification unique des Dispositifs Médicaux (IUD)
Publié le mercredi 6 juillet 2022
Ce que vous devez savoir sur l’UDI ( Unique Device Identifier, en anglais)

UDI (en anglais) ou IUD (en français) est un système d’identification unique des dispositifs médicaux et de leurs accessoires, qui permet d’en assurer la traçabilité. Chaque produit reçoit un numéro d’identification unique. Ce système a pour objectif d’améliorer la sécurité des patients et d’optimiser les soins dispensés, en évitant les erreurs médicales et en participant à l’interopérabilité des applicatifs métiers.
Il vise également à faciliter la surveillance et la traçabilité des dispositifs médicaux, quel que soit le lieu de fabrication ou d’utilisation.
Ce système de standard unique et international est perçu comme fondamental pour assurer une sécurité efficace d’utilisation des dispositifs médicaux (DM) et de leurs accessoires
Tous les DM et DM IV (in vitro) sont concernés, y compris leurs accessoires en Europe. L’UDI devra être utilisé sur l’ensemble de la chaine d’approvisionnement, dès la sortie de production jusqu’à son utilisation, notamment en unité de soin.
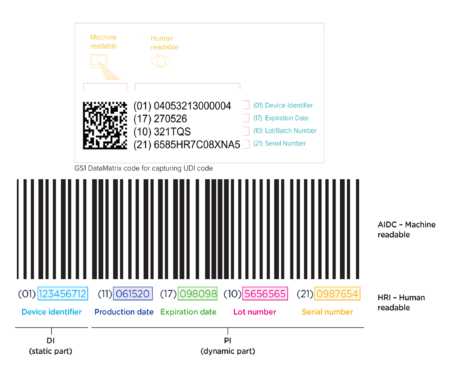
L’élément entièrement nouveau du MDR (règlement relatif aux dispositifs médicaux (UE) 2017/745) est l’UDI. Il prendra la forme d’un code-barres, d’un QR code ou tout autre code lisible par machine et compatible avec d’autres systèmes d’authentification déjà utilisés.
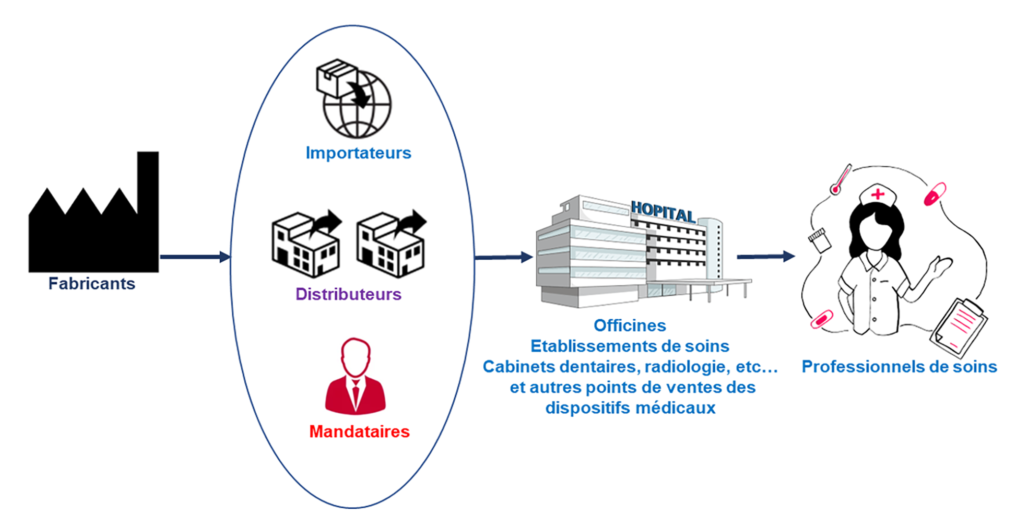
Qui est concerné par l’UDI
-
Les fabricants des dispositifs médicaux
-
Les Distributeurs
-
Les Mandataires
-
Les importateurs
-
Les Officines, établissements de soins, cabinets dentaires, radiologie, etc….
-
Les professionnels de santé
Exemple d’UDI
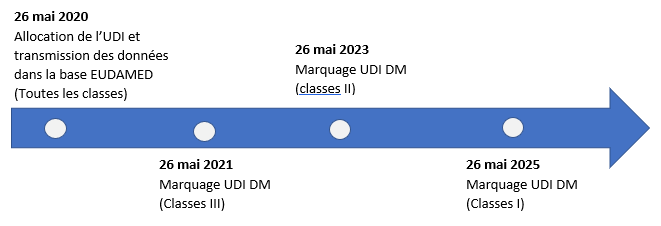
Délai de mise en œuvre en Europe de l’UDI
ARIAQ vous accompagne dans votre processus d’identification et de mise à niveau
Il est capital de correctement planifier votre transition, La formation à ce système d’identification est déterminante.
Faites-vous accompagner et commencez par identifier les changements. Contactez-nous pour en discuter. Au plaisir d’en parler avec Vous !

Formation et conseil en dispositifs médicaux
Ingénieur trinational diplômé en Management des projets Mécatroniques (Suisse – France -Allemagne). Max Ekobe est spécialisé dans la fabrication de dispositifs médicaux stériles et de produits pharmaceutiques. Certifié BSI Lead Auditor ISO 13485. Max a plus de 15 ans d’expérience professionnelle au sein de fabricants internationaux de dispositifs médicaux stériles et de produits pharmaceutiques pour lesquels il a occupé des fonctions d’expert en validation des procédés de fabrication, de chef de projet, responsable ingénierie et responsable des opérations et Qualité. Il a durant sa carrière, géré des projets complexes et pluridisciplinaires.
« Newsletters plus anciennes | Newsletters plus récentes »


















